Vorasidenib在治疗具有易感 IDH1 或 IDH2 突变的 2 级星形细胞瘤或少突胶质细胞瘤疗效如何?
2024 年 8 月 6 日,美国食品药品监督管理局 (FDA) 批准了异柠檬酸脱氢酶-1 (IDH1) 和异柠檬酸脱氢酶-2 (IDH2) 抑制剂 vorasidenib (Voranigo, Servier Pharmaceuticals LLC),用于手术(包括活检、次全切除术或大体全切除术)后患有 2 级星形细胞瘤或具有易感 IDH1 或 IDH2 突变的少突胶质细胞瘤的成人和 12 岁及以上儿童患者。

这是 FDA 首次批准对具有易感 IDH1 或 IDH2 突变的 2 级星形细胞瘤或少突胶质细胞瘤患者进行全身治疗。
在 INDIGO (NCT04164901) 一项随机、多中心、双盲、安慰剂对照研究 INDIGO () 中,对 331 例手术后具有易感 IDH1 或 IDH2 突变的少突胶质细胞瘤患者进行了疗效评估。患者以 1:1 的比例随机接受 vorasidenib 40 mg 口服,每天一次或安慰剂,每天口服一次,直至疾病进展或不可接受的毒性。IDH1 或 IDH2 突变状态由 Life Technologies Corporation Oncomine Dx 靶点测试前瞻性确定。随机分配至安慰剂组的患者在记录到影像学疾病进展后被允许交叉使用 vorasidenib。既往接受过抗癌治疗(包括化疗或放疗)的患者被排除在外。
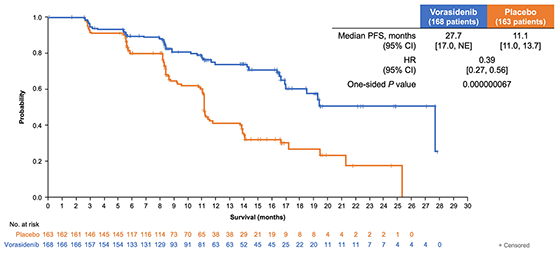
主要疗效结局指标是盲法独立审查委员会,根据修改后的低级别神经胶质瘤反应评估 (RANO-LGG) 标准,使用盲法独立审查委员会。另一个疗效结局指标是下一次干预的时间。PFS 的风险比 (HR) 为 0.39 (95% 置信区间 [CI] 0.27、0.56,p 值< 0.0001)。vorasidenib 组未达到下一次干预的中位时间,安慰剂组为 17.8 个月 (HR 0.26;95% CI 0.15, 0.43, p < 0.0001)。
最常见的 (≥15%) 不良反应是疲劳、头痛、COVID-19 感染、肌肉骨骼疼痛、腹泻、恶心和癫痫发作。最常见的 3 级或 4 级实验室异常 (>2%) 是丙氨酸氨基转移酶升高、天冬氨酸氨基转移酶升高、GGT 升高和中性粒细胞减少。
成人患者的推荐 vorasidenib 剂量为 40 mg,口服,每日一次,直至疾病进展或出现不可接受的毒性。12 岁及以上儿科患者的推荐 vorasidenib 剂量基于体重:体重≥ 40 kg 的患者:40 mg,口服,每日一次。体重 < 40 kg 的患者:20 mg,口服,每日一次。
免责声明
由本文所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考,医康行不承担任何责任。

扫码实时看更多精彩文章
