莫博替尼(mobocertinib)治疗外显子20突变的非小细胞肺癌如何?
正在进行的1/2期临床试验的结果导致美国食品和药物管理局(FDA)对Exkivity(mobocertinib)的“突破性疗法指定”,并最终完全批准该药物。美国FDA授予突破性疗法称号,以加速旨在治疗严重或危及生命的疾病的研究药物的开发和监管审查。具有此名称的药物已显示出初步临床证据,表明该药物可能在一个或多个具有临床意义的终点上表现出比现有疗法的实质性改善。

关于EGFR外显子20插入突变型NSCLC
在美国和欧洲,大约10-15%的非小细胞肺癌(NSCLC)患者,以及亚洲30-40%的患者患有表皮生长因子受体突变(EGFRm)NSCLC。这些患者对称为EGFR-酪氨酸激酶抑制剂(TKI)的精准癌症药物治疗特别敏感,这些药物阻断了驱动表达EGFR的肺癌细胞生长的细胞信号通路。EGFR外显子20插入突变发生在1%至2%的NSCLC中,具有这些突变的患者通常对可用于治疗大多数EGFRm NSCLC的TKI治疗反应不佳。 外显子 20 突变的预后比其他 EGFRm 差,因为目前没有 FDA 批准的治疗方法,并且当前的 EGFR TKI 和化疗对这些患者的益处有限。
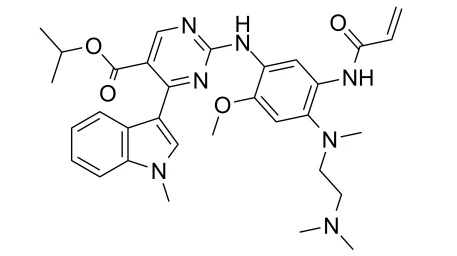
关于Exkivity(莫博丝替尼-TAK-788)
Exkivity 是一种小分子酪氨酸激酶抑制剂,旨在选择性靶向 EGFR 和人 EGFR 2 (HER2) 外显子 20 插入突变。FDA的突破性疗法名称基于一项1期/2期研究的结果,该研究评估了莫西替尼对肿瘤携带EGFR外显子20插入突变且以前接受过全身化疗的局部晚期或转移性NSCLC患者的疗效和安全性。
正在进行的莫博西替尼在既往治疗患者中的1/2期试验结果显示,莫博西替尼在局部晚期或转移性EGFR外显子43插入突变型NSCLC患者中的总缓解率为20%。
20 年国际肺癌研究协会 (IASLC) 2020 年世界肺癌大会 (WCLC) 更新了对接受莫博替尼治疗的 EGFR 外显子 2022 插入阳性 NSCLC 铂类预处理患者的分析。总体而言,35%的人对治疗的反应平均持续17.5个月。
EGFR外显子20插入+NSCLC患者约占NSCLC患者的1-2%,与西方人群相比,该疾病在亚洲人群中更为常见。
莫博司替尼耐受性良好,最常见的副作用是腹泻、恶心、皮疹和食欲下降。与阿米凡他单抗类似,皮疹和指甲变化是常见的皮肤毒性。关于心脏毒性,11%的患者发生QTc延长(>3级,3%),心力衰竭导致1例治疗相关死亡。
免责声明
由本文所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考,医康行不承担任何责任。

扫码实时看更多精彩文章
