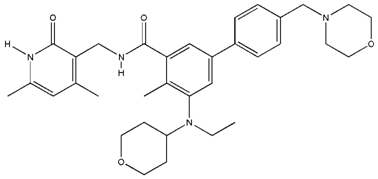
什么是他泽司他(达唯珂®/Tazverik®)?
Tazemetostat(Tazverik™), 一种首创的 zeste 同源物 2 (EZH2) 抑制剂小分子增强剂,于2020年1月在美国获得加速批准,用于治疗年龄≥16岁的成人和青少年,患有局部晚期或转移性上皮样肉瘤,不符合完全切除条件。由Epizyme与Eisai合作开发,这是第一种在美国被批准专门用于治疗上皮样肉瘤的疗法。建议的剂量方案为每天两次,每次800 mg,口服或不口服,直到疾病进展或出现不可接受的毒性。Tazemetostat也正在世界各国进行临床开发,用于其他几种肿瘤类型,包括弥漫性大B细胞淋巴瘤和间皮瘤,美国食品和药物管理局接受了一项新药申请,并优先审查其用于治疗滤泡性淋巴瘤。

他泽司他(达唯珂®)是如何发挥作用的?
azemetostat(Tazverik)是美国食品药品监督管理局(FDA)批准的第一种口服EZH2抑制剂,用于FL和上皮样肉瘤(ES)。在FL中,由于突变体EZH2和WT EZH2与癌基因的相互作用,EZH2活性升高。Tazemetostat抑制FL中的突变体和WT EZH2(Epizyme,股份有限公司,)。此外,他zemetostat抑制一些EZH2功能获得突变,包括Y646X和A687V。
这种抑制抑制抑制B细胞淋巴瘤的增殖,突变体EZH2具有更大的活性(Epizyme,股份有限公司,)。另一方面,ES可以通过SWI/SNF复合物成员的功能障碍,特别是在INI1、SMARCB1或两者缺失的情况下,对EZH2产生致癌依赖性。除了抑制EZH2外,他齐美司他还可以抑制EZH1活性。
作为一种口服药物,他齐司他具有33%的生物利用度。Tazemetostat通过CYP3A进行肝代谢,形成其两种主要的无活性代谢产物M5(EPZ-6930)和M3(EPZ006931),而M5通过CYP3A进一步代谢。这说明了与他司他药物之间的相互作用。他齐美司他的平均终末半衰期为3.1小时,主要通过粪便(79%)和尿液(15%;)排出。
他泽司他(达唯珂®)的效果如何?
一项I期临床试验是第一个确定他泽美司他安全性和剂量的试验。该试验包括 21 例复发/难治性 (R/R) B 细胞非霍奇金淋巴瘤患者和 43 例不符合批准治疗条件或已进展的局部晚期/转移性实体瘤患者。在淋巴瘤队列中,诊断包括 DLBCL (62%) 和 FL (33%)。对于坚实的队列,23% 为 INI1 阴性,7% 为 SMARCA4阴性。
临床结果发现,38% 的淋巴瘤患者的客观缓解率 (ORR),首次缓解的中位时间为 3.5 个月。从第一次反应到疾病进展或死亡的中位反应持续时间为 12.4 个月。相反,在实体瘤队列中,ORR为5%的患者,这仅发生在INI1或SMARCA4阴性疾病的患者中。当观察 INI1 或 SMARCA4 阴性患者时,该亚群中有 38% 具有临床益处,定义为疾病稳定或更好。
上皮样肉瘤
根据对 62 例经组织学证实的局部晚期或转移性 ES 患者进行的 II 期试验结果,Tazemetostat 首次被批准用于 INI1/SMARCB1 功能丧失的 ES。根据 I 期试验的临床结果,患有这种肿瘤的患者需要记录 INI1 表达缺失、双等位基因SMARCB1改变或两者兼而有之。
15%的患者达到了客观缓解的主要终点,根据研究者的评估,所有这些患者都是部分缓解。与I期试验类似,中位缓解时间为3.9个月;然而,未达到中位缓解持续时间。在 12 个月时,21% 的患者无进展生存期,中位生存期为 5.5 个月。在数据截止时,50% 的患者已经死亡,中位总生存期为 19.0 个月。
滤泡性淋巴瘤
根据另一项II期试验的结果,他泽司他第二次获批用于R/R FL 和 FL EZH2 突变体。有 99 名患者每天两次接受 800 毫克剂量,其中 45 名有 EZH2 突变,54 名是 EZH2 WT。该药物一直持续到疾病进展、不可接受的毒性或长达 2 年的治疗。超过 2 年,患者可以在翻转研究中继续治疗。
EZH2突变患者的ORR为69%,而EZH2 WT队列的缓解率为35%。98% 的突变队列和 65% 的 WT 队列观察到肿瘤体积减少。与WT队列相比,突变队列的中位缓解持续时间在数值上更短(10.9个月 vs. 13.0个月),尽管这没有统计学意义。同样,中位持续时间与I期试验相似:两个队列均为3.7个月。6.7% 的 EZH2 突变体和 14.8% 的 WT 患者在整整 2 年内接受治疗,并参加了翻转研究。EZH2突变体和WT队列的中位无进展生存期分别为13.8个月和11.1个月。
总结
作为同类首创的EZH2抑制剂,他泽司他为血液系统和实体恶性肿瘤患者提供了新的口服治疗选择。在血液系统恶性肿瘤中,它被批准用于既往接受过至少两种全身治疗的 EZH2 突变的 R/R FL 患者,以及没有令人满意的替代治疗选择的 R/R FL 患者。对于实体恶性肿瘤,他泽司他已获得 FDA 批准用于 16 岁及以上患有转移性或局部晚期 ES 且不符合完全切除条件的成人和儿童患者。这些适应症是在加速批准的基础上批准的,并取决于确证性试验的临床获益。
总之,他泽司他是一种新型 EZH2 抑制剂,在临床试验中已被证明是有效和安全的,具有可耐受的副作用。然而,他泽司他只是靶向表观遗传调节因子的开始。EZH2已被证明参与许多其他实体瘤和淋巴瘤的肿瘤过程)。
Tazemetostat 以及目前正在临床试验中的其他 EZH2 抑制剂正在研究 DLBCL、套细胞淋巴瘤、前列腺癌、间皮瘤、尿路上皮癌和横纹肌样肿瘤等。其他EZH2抑制剂很可能在不久的将来获得批准。除了单独的 EZH2 抑制剂治疗外,目前正在进行联合治疗的 EZH2 抑制剂和其他疗法(包括免疫疗法、常规化疗和靶向疗法)的临床试验。EZH2抑制剂与免疫疗法或常规化疗相结合,甚至可能显示出协同效应。鉴于 EZH2 抑制的疗效和可耐受的副作用,他泽司他可能是 FDA 批准的更多 EZH2 抑制剂中的第一个。
免责声明
由本文所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考,医康行不承担任何责任。

扫码实时看更多精彩文章
