Belzutifan\贝组替凡与依维莫司在既往治疗过的晚期肾细胞癌中的疗效
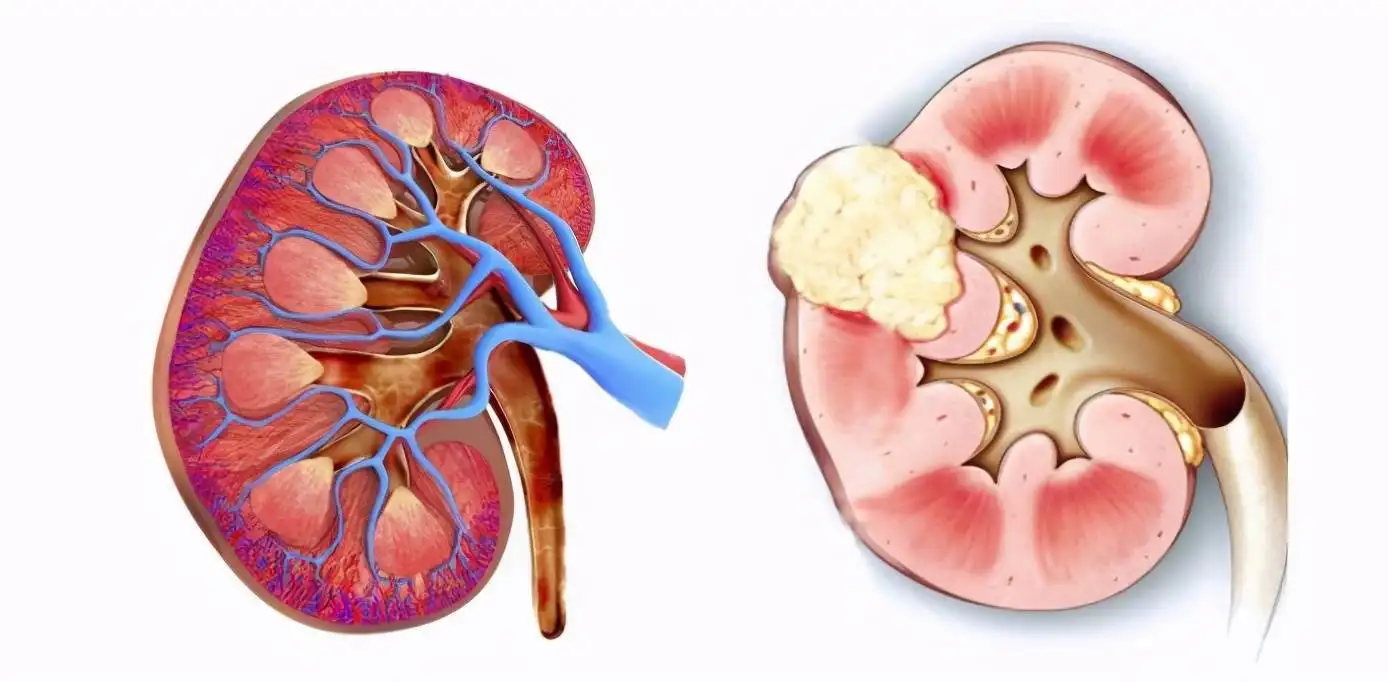
在临床数据III 期 LITESPARK-005 试验显示,与依维莫司相比,缺氧诱导因子-2α 抑制剂 belzutifan 在既往接受过治疗的晚期透明细胞肾细胞癌患者中的无进展生存期有所改善。
研究详情
在开放标签试验中,来自 6 个地区地点的 746 名接受免疫检查点抑制剂 (ICI) 治疗和抗血管生成治疗的患者在 2020 年 3 月至 2022 年 1 月期间被随机分配接受 120 毫克 (n = 374) 的 belzutifan 或 10 毫克 (n = 372) 的依维莫司,每天一次,直至进展或不可接受的毒性。主要终点是无进展生存期和总生存期。
治疗结果
在中位随访 18.4 个月的第一次中期分析中,belzutifan 组的中位无进展生存期为 5.6 个月 (95% 置信区间 [CI] = 3.9-7.0 个月),而依维莫司组为 5.6 个月 (95% CI = 4.8-5.8 个月);18 个月时的发生率分别为 24.0% 和 8.3% (P = .002,满足预先设定的显着性标准)。6 个月时的比率分别为 46.6% 和 42.5%,12 个月的比率分别为 33.4% 和 17.1%。
共有 47.3% 的 belzutifan 组和 64.5% 的依维莫司组接受了后续的抗癌治疗。在中位随访 25.7 个月的总生存期第二次中期分析中,belzutifan 组的中位总生存期为 21.4 个月 (95% CI = 18.2-24.3 个月),而依维莫司组为 18.1 个月 (95% CI = 15.8-21.8 个月);18 个月时的发生率分别为 55.2% 和 50.6% (HR = 0.88,95% CI = 0.73-1.07,P = .20,不符合预先设定的显着性标准)。
在 belzutifan 组的 21.9% (95% CI = 17.8%–26.5%) 与依维莫司组的 3.5% (95% CI = 1.9%-5.9%) 中观察到客观反应 (P < .001)。

不良事件
belzutifan 组发生 ≥ 级 3 级不良事件的比例为 61.8%,依维莫司组为 62.5%;最常见的是 belzutifan 组的贫血 (32.5%) 和缺氧 (10.5%),依维莫司组的贫血 (18.1%) 和高血糖 (5.6%)。严重不良事件发生率为 42.2% vs 38.1%。不良事件导致停止治疗的比例分别为 5.9% 和 14.7%。belzutifan 组 13 例 (3.5%) 发生 5 级不良事件,依维莫司组 19 例 (5.3%) 发生;Belzutifan 组 1 例患者 (0.3%) (由于多器官功能障碍综合征)和依维莫司组 2 例患者 (0.6%) (由于败血症和急性肾损伤)的死亡被认为与治疗有关。
研究人员得出结论:“Belzutifan 在既往接受过免疫检查点和抗血管生成治疗的晚期透明细胞肾细胞癌参与者的无进展生存期和客观反应方面显示出优于依维莫司的显着益处。Belzutifan 没有与新的安全信号相关联。
免责声明
由本文所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考,医康行不承担任何责任。

扫码实时看更多精彩文章
