恩诺单抗(Padcev)的效果如何?特殊人群如何用药?
什么是尿路上皮癌?
当形成膀胱的细胞开始失控地增殖时,膀胱癌就会发展。当其他癌细胞生长时,肿瘤就会出现,随着时间的推移,肿瘤可能会扩散到身体的其他部位。最典型的膀胱癌类型是尿路上皮癌。尿路上皮癌几乎总是患者所患的膀胱癌类型。尿路上皮细胞排列在输尿管、膀胱、尿道、肾盂和其他几个器官中,是癌症最先发生的地方。移行细胞是尿路上皮细胞的另一个名称。这些细胞可以拉伸和改变它们的形状而不会分解。尿路上皮癌也称为移行细胞癌。肾盂是肾脏中与输尿管和尿道相连的部分,全部由尿路上皮细胞衬里。需要检查整个泌尿道是否有肿瘤,因为膀胱癌患者偶尔也会在这些部位发现肿瘤。
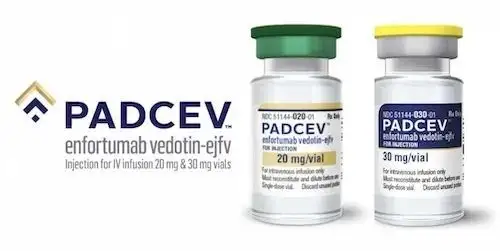
恩诺单抗(Padcev)的作用机制
一种称为 Enfortumab vedotin 的抗体-药物组合由多个部分组成。单甲基奥瑞他汀 E (MMAE) 是一种化疗性微管破坏药物,与一种针对 Nectin-4 的全人源单克隆抗体有关,Nectin-4 是一种在尿路上皮恶性肿瘤中显着表达的细胞外粘附蛋白。可被蛋白酶分解的接头连接这两个部分。表达 Nectin-4 的细胞与 Enfortumab vedotin 结合,产生的 Enfortumab-Nectin-4 复合物被细胞内化。当单甲基奥瑞他汀 E (MMAE) 从细胞内的 Enfortumab vedotin 中释放出来时,细胞的微管网络被破坏,细胞周期被阻滞,最终导致细胞凋亡。
药效 学
一种名为Enfortumab vedotin的抗癌药物通过阻止肿瘤细胞复制来杀死肿瘤细胞。尽管 Enfortumab vedotin 尚未在该人群中进行测试,但既往 MMAE 或含单甲基奥瑞他汀 E 的抗体-药物偶联物显示,中度至重度肝功能损害患者的副事件发生率升高。这些患者不应使用 Enfortumab vedotin。血糖水平高于 250 mg/dl 的患者不应使用 Enfortumab vedotin,因为它有可能诱发严重的高血糖症,在某些情况下还可能诱发糖尿病酮症酸中毒。
临床试验结果:
由于临床试验中的不良反应发生率是在各种不同情况下确定的,因此它们不能直接与其他药物临床试验中的不良反应发生率进行比较,并且可能无法准确代表实际临床实践中的不良反应发生率。警告和预防措施部分包括来自研究的680名暴露于该药物的患者。在接受该药物的680名患者中,有36%的患者暴露时间超过六个月,而9%的患者暴露时间不到12个月。天冬氨酸转氨酶升高、葡萄糖升高、肌酐升高、疲劳、周围神经病变、食欲下降、血红蛋白降低、腹泻、钠下降、恶心、瘙痒、磷酸盐降低、味觉障碍、丙氨酸氨基转移酶升高、贫血、白蛋白降低、中性粒细胞减少和皮疹是该人群中最常见的不良反应。
患有局部晚期或转移性尿路上皮癌的患者,接受过至少一剂 Enfortumab vedotin 并且之前接受过 PD-1 或 PD-L1 抑制剂治疗,以及铂类化疗,被纳入研究以评估 Enfortumab vedotin 的安全性。暴露于该药物的中位时间为 5 个月。在接受该药物的个体中,有47%发生了严重的不良事件。尿路感染、急性肾损伤和肺炎是最常见的主要不良反应。3%的患者发生致命不良事件,包括盆腔脓肿、多器官衰竭、肝功能障碍、脓毒性休克、高血糖和肺炎。17%的患者出现不良反应,导致停药;皮疹和周围神经病变是其中最典型的。61%的患者出现不良反应,需要中断剂量;其中最常见的是疲劳、皮疹和周围神经病变。34%的患者经历了需要减少剂量的不良事件;最常见的此类事件是周围神经病变、皮疹、食欲下降和疲劳。
药物相互作用 - 其他药物对 Enfortumab Vedotin 的影响
同时使用强效 CYP3A4 抑制剂和双重 P-gp 可能导致暴露于非偶联 MMAE 增加,这可能导致 Enfortumab vedotin 毒性的频率或严重程度增加。当 Enfortumab vedotin 与双 P-gp 和强效 CYP3A4 抑制剂同时使用时,应密切观察患者的毒性症状。
该药物在特定人群中的使用:
1、肝功能不全患者
中度至重度肝功能损害患者不应使用 Enfortumab vedotin,因为他们尚未接受药物测试;只有一小部分中度肝功能损害患者被研究。在另一种含有MMAE的抗体-药物偶联物中,中度或重度肝功能损害患者比肝功能正常的患者经历了更多的3级不良事件和死亡。当对轻度肝功能损害的患者施用Enfortumab vedotin时,无需改变起始剂量。
2、肾功能不全患者
轻度、中度或重度肾功能损害患者不需要调整剂量。
3、孕妇
当给予孕妇时,根据其作用方式和在动物身上看到的结果,该药物有可能伤害胎儿。目前尚无关于孕妇药物使用的人体研究可用于确定药物的潜在风险。在一项动物繁殖研究中,Enfortumab vedotin-ejfv 在器官发生期间被施用于怀孕的大鼠,在母体暴露于与推荐人类剂量大致相当的母体暴露时,它会导致母体毒性、胚胎-胎儿致死、结构畸形和骨骼异常。
在器官发生阶段妊娠第 6 天和第 13 天胚胎-胎儿发育的大鼠试验研究中,对怀孕大鼠给予 Enfortumab vedotin-ejfv。在母体致死剂量下,所有怀孕的大鼠都失去了整窝。大约相当于授权人体水平的暴露剂量会导致解剖畸形,例如腹裂、后肢旋转不良、前爪不存在、内脏错位和颈弓融合,以及母体毒性和胚胎-胎儿死亡。此外,还存在胎儿体重减轻和骨骼异常,如不对称、融合、不完全骨化和畸形胸骨、颈弓变形和胸中央单侧骨化。
4、哺乳期患者
没有关于Enfortumab vedotin-ejfv在母乳中的存在、对母乳喂养婴儿的影响或对产奶量的影响的信息。建议哺乳期母亲在使用 Enfortumab vedotin 治疗期间以及最终剂量后至少三周内不要母乳喂养,因为哺乳婴儿可能会发生重大不良事件。
5、性活跃的女性和男性
女性:
妊娠检测:
在开始用药之前,检查具有生殖潜力的女性的怀孕状况。
避孕:
当给孕妇服用时,该药物会伤害胎儿。应建议有能力怀孕的女性在接受药物期间和最终剂量后的两个月内采取有效的避孕措施。
男性:
应建议男性患者在使用该药物时使用可靠的避孕措施,如果他们有能够怀孕的女性伴侣,则在最后一次给药后四个月内使用可靠的避孕措施。动物研究的观察表明,该药物可能会降低男性的生育能力。
6、老年患者
在临床试验中接受药物治疗的680名患者中,年龄在75岁或以上。在这些患者和年轻患者之间,安全性或有效性没有普遍变化。
7、儿科患者
Enfortumab vedotin 尚未被证明对儿科患者安全或有益。
免责声明
由本文所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考,医康行不承担任何责任。

扫码实时看更多精彩文章
